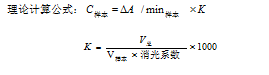乳酸脱氢酶测定试剂盒(乳酸底物法)使用说明书
[产品名称]
通用名称:乳酸脱氢酶测定试剂盒(乳酸底物法)
英文名称:Lactate Dehydrogenase Kit(L-Lactate Substrate Method)
英文简称:LDH Kit
[包装规格]
剂型:液体双剂型
R1:80ml×3 R2:72ml×1
R1:60ml×3 R2:54ml×1
R1:60ml×2 R2:18ml×2
R1:45ml×3 R2:40ml×1
R1:5ml×1 R2:1.5ml×1
[预期用途]
本产品用于体外定量测定人血清中乳酸脱氢酶的活性。
乳酸脱氢酶(Lactate dehydrogenase,LDH,E.C.1.1.1.27)是由心型(H)和肌型(M)两亚基组成的四聚体,人体内有五种同工酶(LDH1~LDH5),分子量为34000。在高氧耗的组织中H型亚基占主导,如心肌组织中的LDH1约占LDH总活力的50%;在高糖酵解的组织中M型亚基占主导,如横纹肌中以LDH5为主,而在脾和肺组织中以LDH3为主。
临床上测定血液中LDH的活性,常用于诊断心肌梗死、肝和骨骼肌的疾病。
临床检测乳酸脱氢酶指标常用的方法有两种:①以乳酸和NAD+为底物,从乳酸氧化成丙酮酸的正向反应,称乳酸底物法;②以丙酮酸和NADH为底物,从丙酮酸还原成乳酸的逆向反应,称丙酮酸底物法。本产品即以其中的乳酸底物法为反应原理,此检测方法试剂稳定性好,保持线性速率反应的时间范围较宽,重复性好[1, 2]。
[检验原理]
乳酸脱氢酶催化L-乳酸到丙酮酸的正向脱氢反应,使氧化型辅酶Ⅰ(NAD+)还原生成还原型辅酶Ⅰ(NADH),引起340nm波长处吸光度的升高;吸光度的升高与血清中乳酸脱氢酶的活力成正比。反应式如下:
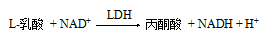
[主要组成成份]

说明:
不同批号的试剂不能混用;新打开的试剂不宜与已用过的试剂混合在一起,否则易造成试剂稳定性下降。
[储存条件及有效期]
1.原包装试剂在2℃~8℃避光贮存,有效期12个月。
2.试剂开盖后在2℃~8℃避光保存,稳定期30天。
[适用仪器]
本试剂盒适用于HITACHI 7180/7170/7060/7080/7600P、OLYMPUS AU 400/600/640/2700/5400 、BECKMAN COULTER CX5 、BECKMAN DXC-800、TOSHIBA 40FR/120FR全自动生化分析仪和各种半自动生化分析仪。
[样本要求]
1.样本种类:新鲜无溶血血清。
2.样本采集:常规静脉采血约3ml,置于玻璃试管中,样本采集后,立即密封送检,严格避免溶血[3]。
3.样本干扰:对反应吸光度有干扰的样本,包括溶血和浑浊的样本都可能影响检测结果,遇上述情况建议重新采集。
4.样本保存:样本2℃~8℃可稳定3天,忌冻融。
[检测方法]
1.试剂的准备:试剂开瓶即可使用。
2.检测步骤:
(1)全自动生化分析仪操作步骤:
基本操作步骤:(波长:340nm 温度:37℃ 比色杯光径:1cm)
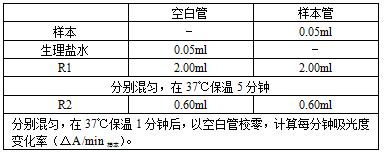
上机操作步骤:参数设置→试剂装载→校准→质控→样本加载→测定→结果审核→报告。
(2)半自动生化分析仪操作步骤:先将R1和R2按照10:3的比例混匀配制成工作液,然后将工作液和样本按照65:2的比例混匀,上机测定。
3.校准:使用K因数校准,也可使用Roche校准品校准;当试剂更换批号、质控出现漂移、仪器做完保养、重要零件更换时应重新进行校准。
4.质量控制:每天对样本进行检测之前,须进行质量控制,以保障测试系统的稳定性。建议采用本公司生化多项质控品或Roche质控品进行室内质控,质控品测定结果应在允许范围内。若超出质控范围,需查找原因,如仪器、试剂与质控品的状态或参数设置等。
5.检验结果的计算:生化分析仪会自动给出检测结果。
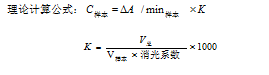
NADH在340nm波长下毫摩尔分子消光系数为6.3。
[参考范围]
根据参考文献[2]获得以下参考范围:
健康成人为109U/L~245U/L。
各医院应根据本地区实际情况建立自己的参考范围。
[检验结果的解释]
专业人员负责检验结果的审核。检验结果会受到受检者年龄、性别、体重等的影响。通常情况下,其结果如在参考范围内,认为正常;如在临界区域内,应重新测定进行确认;如明显超出参考范围或确认检测后仍超出参考范围,则认为血清LDH活性异常。检验结果如出现与临床不符甚至相悖的情况,应分析与查找原因。
[检验方法的局限性]
1.乳糜(Intralipid)≤1000mg/dl时,对测定结果没有明显干扰。
2.溶血对测定结果有干扰,样本应严格避免溶血。
3.Vc≤100mg/dl时,对测定结果没有明显干扰。
4.胆红素≤40mg/dl时,对测定结果没有明显干扰。
5.检测结果与所使用的仪器种类、型号和校准品相关,使用不同的仪器或校准品,检测结果可能会有差异。
[产品性能指标]
1.外观:a) R1应为无色透明溶液,无杂质、无絮状物,外包装完整无破损。b) R2 应为无色透明溶液,无杂质、无絮状物,外包装完整无破损。
2.试剂空白吸光度:在波长340nm(光径1cm)处,试剂空白吸光度(A)应≤0.600;试剂空白吸光度变化率(△A/min)≤0.003。
3.准确度:
出厂检验:测定Roche质控品,测定值与标示值的相对偏差应不超过±15%。
型式检验:测定国家标准物质GBW(E)090284或GBW(E)090285,测定结果的相对偏差应不超过±10%。
4.分析灵敏度:活性为200U/L的LDH所引起的吸光度变化率(△A/min)应在0.010~0.050的范围内。
5.重复性:测定值的变异系数(CV)应≤5%。
6.批间差:试剂盒的批间差(R)应≤6%。
7.线性范围:
在5U/L~1000U/L范围内,线性相关系数(r)应≥0.990;
在5U/L~50U/L范围内,线性绝对偏差应不超过±5U/L;
在50U/L~1000U/L范围内,线性相对偏差应不超过±10%。
[注意事项]
1.试剂避免直接接触皮肤和眼睛,切勿吞咽。
2.使用前应该认真阅读产品说明书,使用后的器具须按照相关医疗废弃物的处理规定处理。
3.由于运输过程产生渗液或漏液的产品,或在运输贮存中没有按照说明书要求进行维护的试剂,不可使用。
4.本产品仅适用于临床体外诊断,需专业人员使用。
5.如医院使用其它型号的全自动生化分析仪,请各医院根据实际需要进行验证。
[标签中图标解释]
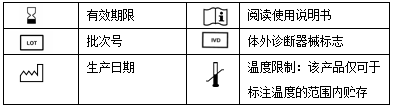
[参考文献]
1.陆永绥、李清华、张伟民主编.临床检验自动化仪器分析标准操作规程.浙江大学出版社.2006.
2.中华人民共和国卫生部医政司.全国临床检验操作规程(第3版).东南大学出版社. 2006.
3.王惠萱、李雪梅、王珂主编.临床检验样本采集手册.云南科技出版社.2008.
[生产企业]
企业名称:中生北控生物科技股份有限公司
注册地址:北京市昌平区科技园区超前路27号
生产地址:北京市昌平区科技园区超前路27号
[医疗器械生产企业许可证编号]
京药监械生产许20000271号
[医疗器械注册证书编号]
京食药监械(准)字2014第2401131号
[产品标准编号]
YZB/京 1736-2013
[说明书批准日期及修改日期]
2014年9月22日






 所有类目
所有类目